Болезнь Паркинсона: фармакотерапевтические аспекты амбулаторно-поликлинического этапа
Резюме
нет
Ключевые слова
Статья
Введение. Сегодня болезнь Паркинсона (БП) неизлечима и набор лекарственных средств ограничен лишь симптоматической терапией. Однако признано, что надлежащее и вовремя начатое лечение благотворно влияет на течение заболевания и, тем самым, экономически целесообразно.
Универсальных правил лечения пациентов с БП не существует, но тем не менее разработаны принципы и алгоритмы терапии, позволяющие реализовать индивидуальный подход в каждом конкретном случае. Известные терапевтические закономерности неоднократно обобщались в работах зарубежных [8, 9] и отечественных [1, 5] паркинсологов и официально были закреплены в России «Протоколом ведения больных с БП» (2005) [2]. Нормативный характер «Протокола» предусматривает обязательное соблюдение неврологами поликлиник его требований при назначении терапии больным.
Основными факторами, определяющими выбор противопаркинсонических препаратов по протоколу, являются возраст больного, степень выраженности двигательных нарушений и наличие когнитивных расстройств. Логическая схема, иллюстрирующая алгоритм назначения лекарственных средств по «Протоколу» представлена на рис. 1.
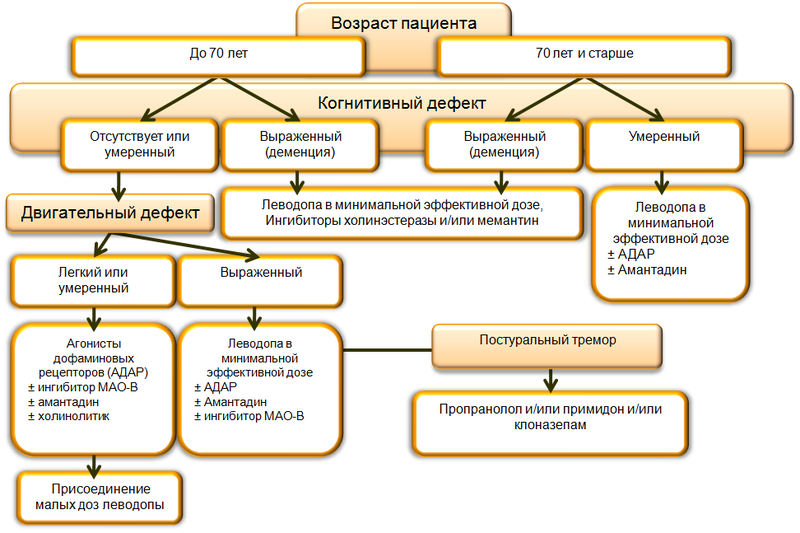

Рисунок 1. Алгоритм терапии болезни Паркинсона
Методы. Фактологическая основа исследования – данные консультативного приема 354 больных с направительным диагнозом болезнь Паркинсона.В 2008–2011 гг. нами осматривались целевые больные, которые в ряде случаев для верификации нозологической формы наблюдались длительное время– до 2–3-х лет. Диагноз БП устанавливался клинически на основе анамнеза и текущего неврологического статуса в соответствии с критериями Банка Головного Мозга Общества БП Великобритании [7], Национального Института Неврологических Расстройств и Инсульта (NINDS USA, 1999) [6] и рекомендаций Американской академии неврологии по диагностике и лечению БП (2006) [1].
Результаты и обсуждение. Анализ терапевтической целесообразности медикаментозных назначений неврологов поликлиникпроведен в соответствии с «Протоколом» у 72,88% (258/354) больных с подтвержденным направительным диагнозом БП, получавших лечение.
Так, при назначении терапии возраст больных не учитывался в 16,67% (43/258) случаев: холинолитики назначались пожилым (35 чел.), а леводопа – относительно молодым (до 50-ти лет) с легкими двигательными нарушениями.
Агонисты дофаминовых рецепторов (АДР) принимали всего лишь 35,66% больных (92/258), и из них чрезвычайно мало – 23,26% (60/258) – на ранних стадиях заболевания и только 12,40% (32/258) на поздних стадиях. И это на фоне заслуженного признания АДР препаратами первого ряда как при монотерапии на ранних стадиях, так и в комбинации с леводопой при выраженных клинических проявлениях [3, 4]. Главной особенностью выбора специалистами поликлиник препаратов из группы АДР стала ограниченность назначений списком ДЛО – дополнительного лекарственного обеспечения – с его безальтернативностью в отношении Пирибедила, при относительной доступности и известных преимуществах других препаратов (Прамипексол и Ропинирол). К тому же 2/5 больным Пирибедил был назначен в субтерапевтических дозах по 50-100 мг/сут. и даже по 25 мг (½ таб.) 1-2 раза в день при обязательном приеме таблетки целиком. Неоправданной была и длительная монотерапия АДР у 41 больного, 24 из которых уже имели выраженные клинические проявления.
Правильность назначений холинолитиков в соответствии с возрастом не превышала ~ 40% (22/57), и все получавшие препараты этой группы длительно находились на монотерапии.
Ингибиторы МАО-В и препараты амантадина неврологами поликлиник не назначались вообще.
Наибольшее количество ошибок допущено при назначении препаратов леводопы, которые принимали 174/258 (67,44%) человек. Раннее, не соответствующее клиническим проявлениям назначение леводопы отмечено у 24,42% (63/258) больных, из них у 3,88% (10/258) человек даже на первой стадии заболевания. Наряду с этим наблюдалось и неоправданно позднее назначение леводопы, более того ~ 7-ми % (18/258) пациентов с выраженными двигательными нарушениями препараты леводопы не назначались. Субтерапевтические дозы (менее 200 мг) принимали 22,09% (57/258) человек с развернутыми клиническими проявлениями болезни. Отмечались даже казуистические случаи приема препаратов леводопы по 62,5 мг 3 раза в день пациентами с 3-4 стадиями заболевания. Неоправданно высокие суточные дозы (1000 – 2000 мг) получали 18,60% (48/258) пациентов, из них 11 человек со 2 стадией заболевания. Кроме того, отмечалась неадекватная кратность приема препаратов леводопы: от 1-2 раз в день по 50 – 125 мг (у 41 человека) до 8-10 раз в день (у 7 человек), и даже до 20 раз в день по 62,5 мг одним пациентом. Встречалась и необоснованная комбинация «оригинальной» леводопы и дженериков у 6,98% (18/258). Наиболее грубой ошибкой являлась внезапная отмена противопаркинсонических лекарственных средств, особенно препаратов леводопы у 9 человек, что сопровождалось декомпенсацией заболевания и даже развитием акинетического криза. Нередко случалась и неоправданная замена одного препарата леводопы на другой, обусловленная трудностями льготного лекарственного обеспечения или региональными фармакоэкономическими аспектами терапии.
Надо сказать, фармакоэкономическая целесообразность назначений препаратов леводопы на амбулаторно-поликлиническом этапе муниципального уровня ограничена применением лишь двухкомпонентных лекарственных средств как в рамках ДЛО, так и при самостоятельном приобретении. При этом по спискам ДЛО 40% (67/174)больных получают заметно отличающийся по качеству дженерикТидомет форте.Периодическая необеспеченность льготников в регионе препаратами ДЛО вынуждает больных покупать этот препарат в розничной аптечной сети. Как альтернативу ему неврологи разумно предлагают практически с одинаковой частотой оригинальные препараты леводопы Наком и Мадопар – 60% (107/174) всех назначений и не обходят вниманием эффективныйдженерикТремонорм.
Приназначении противопаркинсонических препаратов примерно в каждом пятом случае отсутствовал период постепенного наращивания дозы – «титрования» лекарственных средств для предотвращения возможных побочных эффектов.
Выраженность когнитивного дефекта при лечении БП ни у одного больного во внимание не принималась. Характерным было также необоснованное назначение традиционных средств с ноотропным и вазоактивным действием у 79,07% (204/258) пациентов, половина которых (135/258) принимала эти препараты практически постоянно.
Таким образом, терапия БП на амбулаторно-поликлиническом этапе в основном была представлена преобладающим назначением препаратов леводопы 67,44% (174/258) и меньшим почти в два раза назначением Пирибедила. Применение же Тригексифенидила у 22,10% (57/258) больных соответствует современным представлениям об эффекте холинолитиков [1].
В целом прослеживается тенденция увеличения назначений препаратов леводопы от стадии к стадии. И её следовало бы признать соответствующей «Протоколу», если бы не очень раннее назначение препаратов леводопы больным даже на первой стадии. Однако не соответствует общепринятым рекомендациям существующая тенденция в назначении единственного АДР – Пирибедила: невысокий уровень назначений препарата на ранних стадиях болезни, снижающийся по мере её прогрессирования. Уровень назначений Тригексифенидила можно считать приемлемым на каждой стадии за исключением возрастных несоответствий. Надо отметить невысокий удельный вес (~ 30–50%) комбинированной терапии на 1–3 стадиях болезни. Коррекция моторных флуктуаций, лекарственных дискинезий и немоторных проявлений заболевания на амбулаторно-поликлиническом этапе не проводилась.
Заключение. Краткопрокомментируем собственную коррекцию терапевтических назначений амбулаторно-поликлинического уровня неврологической помощи больным с БП. Как правило, в отношении таких больных к моменту обращения на консультативный прием уже не приходилось сомневаться в достоверности клинического диагноза «болезнь Паркинсона». Поэтому врачу с больным предстояло сделать нелегкий выбор в отношении варианта лечения, где определяющим фактором, как известно, является возраст. Если пациент относительно «молод», то выбор терапии, обеспечивающей более высокую двигательную активность в ближайшей перспективе, не самый оптимальный. Поскольку снижение риска развития флуктуаций и лекарственных дискинезий в долгосрочной перспективе для такого больного гораздо важнее. Если же пациент из когорты пожилых, то выбора у него может и не быть. В любом случае терапия для каждого пациента строго индивидуальна, и задача врача – согласовать оптимальность терапевтических решений с рациональностью восприятия больным своей болезни, с его социальным статусом.
В связи с этим всем больным, получавшим Пирибедил из актива ДЛО, была скорректирована суточная доза и кратность приема препарата. Пациентам с легкими и умеренными двигательными нарушениями, не принимавшим АДР, нами по мере возможности назначались Прамипексол или Ропинирол(Реквип Модутаб) в адекватной терапевтической дозе последовательным титрованием. Последний препарат и появившийся в последствии Прамипексол пролонгированного действия (Мирапекс ПД) стали для них настоящим средством выбора, особенно при низкой комплаентности. В отсутствие достаточного эффекта наши больные дополнительно получали амантадин, а при выраженном треморе покоя ещё и Тригексифенидил в терапевтической дозе.
Степень функционального дефекта и индивидуальная восприимчивость каждого конкретного больного послужили значимым основанием для коррекции уже имевшихся и новых назначений препаратов леводопы, которая обычно эффективно сочеталась нами с приемом АДР. В зависимости от финансовой состоятельности пациентов и особенностей регионального рынка противопаркинсонических препаратов практически с одинаковой частотностью для лечения БП выбирались двухкомпонентные препараты леводопы Наком, Мадопар и Тремонорм. Уровень приема современного эффективного трехкомпонентного препарата леводопа/карбидопа/энтакапон(Сталево), несмотря на наши совместные с больными усилия, сегодня едва достигает 10%. Наблюдавшиеся на развернутых стадиях БП неминуемые моторные флуктуации и лекарственные дискинезии корригировались по мере проявления в соответствии с общепринятыми схемами, исключая ингибитор МАО-В. На муниципальном уровне принимать препарат этого класса Разагилин(Азилект)лишь эпизодически смогли себе позволить считанные единицы.
Подобная ситуация складывалась и при назначении Мемантина или трансдермальной формы Ривастигмина(Экселон) у больных с выраженными когнитивными нарушениями. Необходимую терапию в этом случае смогли себе позволить лишь семьи ~ 4% больных и то не постоянно.
Литература
- Левин О.С., Федорова Н.В. Болезнь Паркинсона: монография. 2-е изд. М.: МЕДпресс-информ, 2012; 352 с.
- Протоколведениябольных. БолезньПаркинсона. Проблемы стандартизации в здравоохранении 2005; (3): 74-166.
- Федорова Н.В. Агонисты дофаминовых рецепторов в лечении болезни Паркинсона. В кн.: Болезнь Паркинсона и расстройства движений: Рук. для врачей: по матер. I нац. конгресса. Под ред. С.Н. Иллариошкина, Н. Н. Яхно. М, 2008: 162-170.
- Федорова Н.В. Практические аспекты применения препаратов леводопы в лечении болезни Паркинсона. В кн.: Болезнь Паркинсона и расстройства движений: Рук.для врачей: по матер. II нац. конгресса. Под ред. С. Н. Иллариошкина, О.С. Левина. М, 2011: 180–188.
- Шток В.Н., Федорова Н.В. Болезнь Паркинсона. В кн.: Экстрапирамидные расстройства: Руководство по диагностике и лечению. Под ред. В.Н. Штока, И.А. Ивановой-Смоленской, О.С. Левина. М.: МЕДпресс-информ, 2002. Гл. 5: 94–122.
- Gelb D.J., Oliver E., Gilman S. Diagnostic criteria for Parkinson disease. J Arch Neurol 1999; 56(1): 33–39.
- Gibb W.R., Lees A.J. The relevance of the Lewy body to the pathogenesis of idiopathic Parkinson’s disease. J Neurol Neurosurg Psychiatry 1988; 51(6): 745–752.
- Parkinson's disease and movement disorders. Ed. J. Jankovic, E. Tolosa. 5th ed. Lippincott Willams & Wolters Kluwer, 2007; 720 p.
- Parkinsonian disorders in clinical practice. Edited by A.H.V. Schapira, A. Hartmann, Y. Agid. Blackwell Publishing Ltd., 2008; 192 p.

